尊龙凯时 - 人生就是搏!生物AlfaDAX线上系统()对28个创新分子的聚集沉淀性进行了预测,并用湿实验进行一一验证,有聚集沉淀的分子预测正确率达100%,非聚集沉淀的分子准确率达78.6%,综合评估正确率达89.3%。
通过对6个公开的抗体数据对比,验证了AlfaDAX线上系统可有效帮助客户提前通过分子改造去规避风险,加速推进新药上市进程。

▲AlfaDAX线上系统网址
28个创新分子聚集沉淀预测
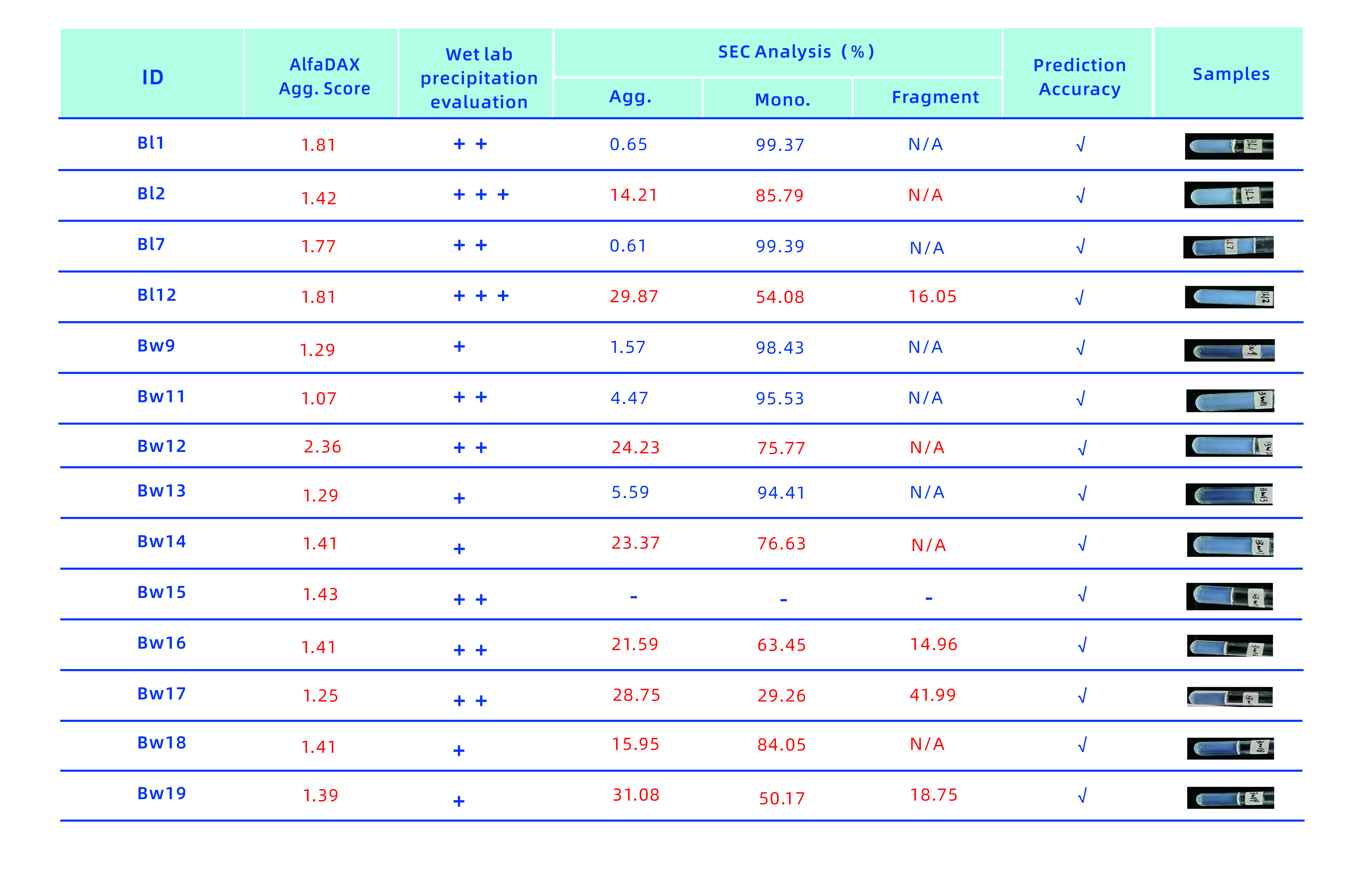
▲图1:预测14个有聚集沉淀的创新分子正确率达100%
如图1所示,AlfaDAX线上系统经过聚集评分后,对14个创新分子进行了标红预警。这14个创新分子稍后进行了湿实验的浑浊度评价和SEC检测,结果都有聚集沉淀。AlfaDAX线上系统预测有聚集沉淀的分子正确率达到100%,提前发现风险,有效减少湿实验的工作量。
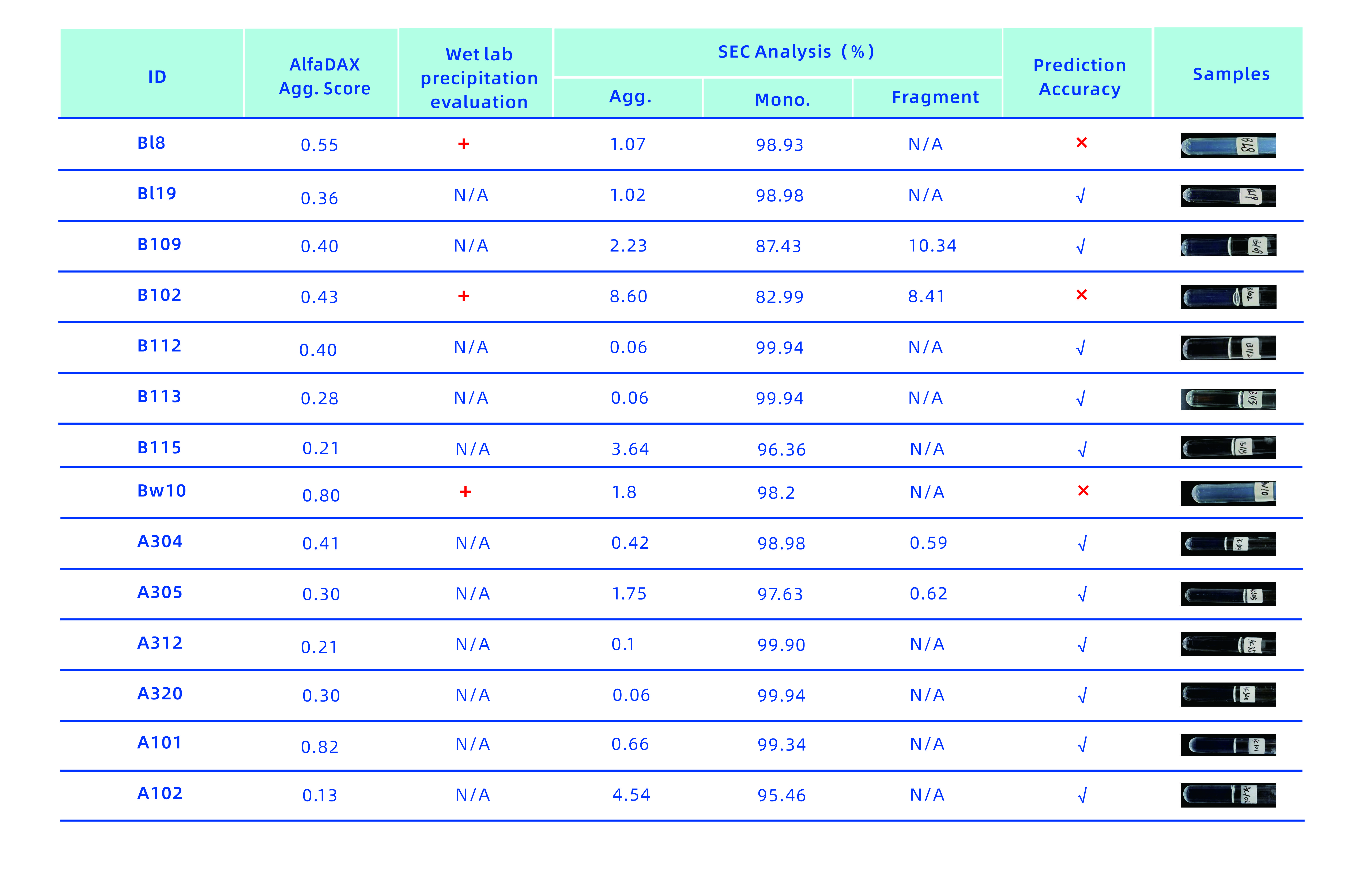
▲图2:预测14个非聚集沉淀的创新分子的正确率达78.6%
如图2所示,AlfaDAX线上系统对另外14个创新分子进行了聚集评分,结果为无聚集沉淀。同样,这14个创新分子也进行了湿实验的浑浊度评价、SEC检测结果,其中11个是无聚集,3个有聚集。AlfaDAX系统坚持不漏掉一个好分子的严谨态度,对非聚集沉淀的分子准确率达78.6%。
6个公开药物分子评估结果
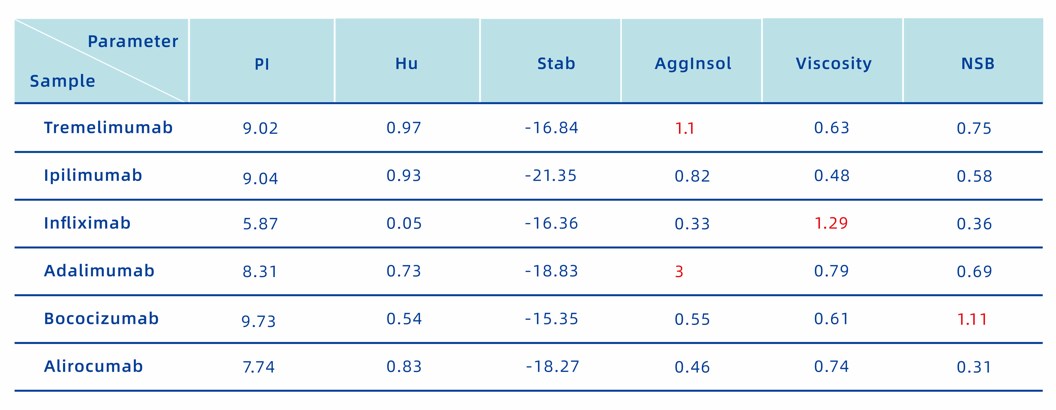
▲图3:6个公开药物分子的评估结果
Tremelimumab和Ipilimumab都是CTLA4的已上市抗体,AlfaDAX线上系统预测Tremelimumab容易聚集,而Ipilimumab不容易聚集,与实际相符[1]。根据报道,目前Ipilimumab比Tremelimumab的确有更广泛的使用,美国FDA于2011年3月25日批准Ipilimumab用于治疗晚期黑色素瘤,适用于无法切除或转移性黑色素瘤、中危或低危晚期肾细胞癌以及特定类型的转移性结直肠癌患者。Tremelimumab多用于转移性黑色素瘤研究,需要与Durvalumab联合使用来治疗肝癌、肺癌等实体癌。
Infliximab与Adalimumab都是TNFα的已上市抗体,不过Infliximab的黏度较高[2]。抗体在高浓度下如果展现出较高的粘度,则在给患者注射时需要更大的推力,更大的针头或者降低浓度分批次注射,增加了患者的痛苦,因此FDA批准Infliximab的最大推荐浓度为4mg/ml[3], 大大地限制了疗效,而Adalimumab的最大推荐浓度可以达到100mg/ml[4],这也是Adalimumab能够销量居高不下的原因之一。虽然全人源的Adalimumab能够被广泛地使用,与鼠源的Infliximab一样,依然会产生比较严重的免疫原性问题,约有28%的患者注射Adalimumab三年内产生抗药性抗体,影响疗效,产生安全问题[5]。原因正如AlfaDAX线上系统所预测的一样,Adalimuamb容易通过静电力相互吸引产生聚集,在搅拌的情况下容易产生不同程度的聚集小颗粒,这些不同程度的聚集小颗粒是引起不同程度的免疫原性的主要原因[5]。
Adalimumab作为全球第一款人源化TNFα单抗,凭借更低的副作用和患者耐药性,上市第一年销售额便达到2.8亿美金。目前阿达木单抗在全球范围内被批准的适应症涉及到类风湿性关节炎、银屑病、等十余种疾病,在中国获批的适应症有8个,均进入2022年国家医保目录。如果Adalimumab的成药性更好,减少因聚集而产生的免疫原性,将能更好地造福患者。

Bococizumab与Alirocumab同样是PSCK9的抗体,用于高胆固醇血症的研究,但Bococizumab在三期临床被叫停,而Alirocumab则成功上市。Bococilizumab具有较强的非特异性结合倾向,从而影响疗效以及产生毒副作用[6],与AlfaDAX线上系统分析一致。bococizumab在降低低密度脂蛋白胆固醇的作用强度上没有达到预期,而且相比其他PCSK9抑制剂有较高的免疫原性和注射部位不良反应,这是非特异性结合差限制了成药性的典型案例。
结 论
AlfaDAX线上系统预测28个创新分子聚集沉淀的正确率达89.3%,帮助客户提前通过分子改造去规避风险,加速推进新药上市进程,欢迎全球生物药物同仁体验、反馈。
参考文献
1.step, P., Caffry, I., Yu, Y., Sun, T., Cao, Y., Lynaugh, H., ... & Xu, Y. (2015, May). An alternative assay to hydrophobic interaction chromatography for high-throughput characterization of monoclonal antibodies. In MAbs (Vol. 7, No. 3, pp. 553-561). Taylor & Francis.
2.Thorsteinson, N., Gunn, J. R., Kelly, K., Long, W., & Labute, P. (2021, January). Structure-based charge calculations for predicting isoelectric point, viscosity, clearance, and profiling antibody therapeutics. In MAbs (Vol. 13, No. 1, p. 1981805). Taylor & Francis.
3.//www.accessdata.fda.gov/drugsatfda_docs/label/2021/103772s5401lbl.pdf
4.//www.accessdata.fda.gov/drugsatfda_docs/label/2023/125057s423lbl.pdf
5.Heljo, P., Ahmadi, M., Schack, M. M. H., Cunningham, R., Manin, A., Nielsen, P. F., ... & Jiskoot, W. (2023). Impact of stress on the immunogenic potential of adalimumab. Journal of Pharmaceutical Sciences, 112(4), 1000-1010.
6.Makowski, E. K., Chen, H., Lambert, M., Bennett, E. M., Eschmann, N. S., Zhang, Y., ... & Tessier, P. M. (2022, December). Reduction of therapeutic antibody self-association using yeast-display selections and machine learning. In MAbs (Vol. 14, No. 1, p. 2146629). Taylor & Francis.